クロマトグラフィーにおける生体分子認識機構と
移動現象の解析による新規分離方法の開発
クロマトグラフィーにおける生体分子認識機構と
移動現象の解析による新規分離方法の開発


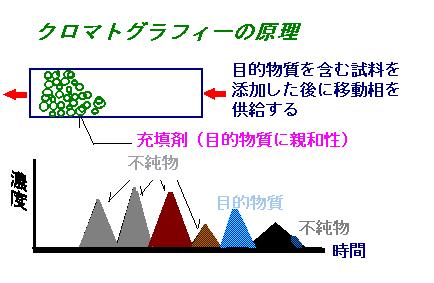
生体分子の分離分析には欠かすことのできないクロマトグラフィーは溶質とカラム固定相との平衡関係(分配係数)で規定される速度でカラム内を移動する間に分離が行われる(移動速度差分離)。分配係数は実は分子認識を反映するものである。従来のクロマトグラフィー研究は、分子認識について詳細に検討せずに単に分配係数として取り扱いゾーン分散(移動)モデルに組み込む工学的解析と、免疫affinityやbioimprintingのように親和性のみを重点的に調査するという2つがほとんどである。
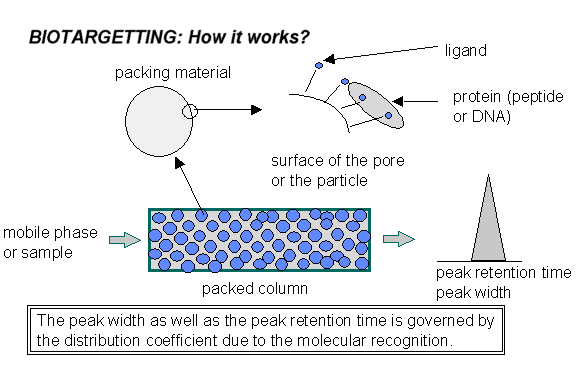
しかしながら、分子認識とゾーン分散(移動速度)は独立ではない。たとえば、リガンドと溶質(以下タンパク質とする)が強い相互作用を持つとタンパク質の吸脱着(拡散)速度は著しく低下する。また、リガンドとタンパク質の結合力に分布があると(不均一リガンド)、吸脱着速度も均一系とは異なる。リガンド、タンパク質、細孔の(相対的)大きさや方向(立体的配置)も重要であるが未だ検討は不十分である。さらに、単一の相互作用による分子認識に加えて他の相互作用が協調的に働くと分離挙動は一層複雑となる。
本研究ではクロマトグラフィーにおける分子認識機構と移動現象(ゾーン分散機構)を同時に解析し、解析結果をフィードバックすることにより新規高分離性能クロマトグラフィーを開発することを目的とする。このようなクロマトグラフィーの用途は、タンパク質およびペプチド医薬品の工業分離プロセス、高性能分析手段、工業分離プロセスにおけるオンラインモニタリングと多岐にわたる。また、分子認識機構に基づく結合定数や解離定数などの生体分子相互作用に関する情報の決定方法としても期待できる。
1 静電気的相互作用(イオン交換)クロマトグラフィー(IEC)における分子認識機構 私たちはIECのタンパク質保持機構(分子認識機構)を調査する有効な方法を開発し、タンパク質は多点でIECゲルと結合し、その結果わずかな塩濃度の変化で吸着が急激に変化すること、正味の電荷ではなく表面電荷分布を分子認識し高度分離ができることをはじめて見いだした。最近提案されている粒子細孔内にリガンドを含むゲルを埋めたコンポジットゲルでは静電気的相互作用に加えてゲルの膨潤・収縮による分子サイズ認識機構が強く働くと考えられる。このような二つの分子認識機構が働くIECについて重点的に調査している。
静電気的相互作用による分子認識の解析:塩濃度勾配溶出実験から溶出塩濃度と規格化した勾配との関係を多くのタンパク質、ペプチド、DNAについて求める。また、イオン交換ゲルとしては通常の多孔性ゲルの他にbase
matrixの細孔内にほとんど架橋されていないゲル(リガンドを含む)を埋め込んだコンポジットゲルや非多孔性粒子、膜状充填剤、一体型成形された充填剤について調査する。
分子の大きさによる分子認識の解析:異なる大きさのタンパク質プローブを用いてサイズ排除曲線を通常の溶出液量からの決定方法とinverse size
exclusion chromatography 法を用いて作成し、移動相のpHあるいは塩濃度の影響について検討する。
分子認識と移動現象の関係:溶出曲線の広がりと分子認識の結果としての分配係数の関係について検討する。また、リガンドの不均一性についても両方への影響について調査する。
2 protein A による抗体分離機構 protein Aクロマトは抗体医薬品の有効な精製方法やimmunoassayとして期待されているが、IECなどの低分子リガンドと比べると、その分離機構は大きく異なる。特にprotein
A,抗体,細孔の大きさと立体的配置に着目して解析している。
Shuichi Yamamoto home page top menuに戻る